カリキュラム、シラバス
令和2年度 AMED中央IRB促進事業
コンピテンシーに基づくアカデミア所属モニターの教育プログラム作成班(研究代表者 山口拓洋)作成
・主に医師主導治験を実施するアカデミア所属モニターの対象
(ただし、AROモニターの状況も踏まえ、一部、研究者主導の特定臨床研究等の内容も加えた)
・演習の手段は、目安として、オンライン研修、集合研修を明記 (情勢によって変更可)
・参考文献は文献や参考資料だけではなく、e-learning等も含む
| カリキュラム・シラバスの構成 | |
| 授業科目 | ACRP Core Competency Framework for Clinical Study Monitoring /Joint Task Force for Clinical Trial Competencyの8つのドメインをもとに、アカデミア所属モニターが受講すべき研修内容を分類 |
| テーマ | 該当するコンピテンシー等 |
| 授業科目の目標 | 習得することが期待されるスキル・技能・態度 |
| 教育方法とコマ数 | 講義、演習別の教育方法と、想定される研修時間(1コマ=60 分) |
| 概要 | 講義、演習それぞれの目標と内容、参考文献等 |
| 備考 (関連するシラバス) |
組み合わせて実施することが望ましい研修のシラバス |
| カリキュラム・シラバスのご利用について 氏名 ・所属 ・連絡先(メールアドレス)・利用目的(研修目的の場合は研修会名もしくは研修対象者) をメール本文に記入し、東北大学ネットワーク事務局(trnw-office(@)crieto.hosp.tohoku.ac.jp)までご連絡ください。 なお、利用目的等によっては、ご利用をお断りすることがあります。 また、ご利用いただく際は、後日、アンケート等をお願いする場合があります。 |
研修資材
令和2年度 AMED中央IRB促進事業
コンピテンシーに基づくアカデミア所属モニターの教育プログラム作成班(研究代表者 山口拓洋)作成
研修で使用する医師主導治験の模擬SDV・模擬文書モニタリング用資材一式を作成(計80種類以上)
模擬SDV用資材
治験実施計画書
同意説明文書
カルテ一式
CRF(未入力・入力済)
SDVチェックリスト(未記入)
重篤な有害事象に関する報告書(未記入)
重篤な有害事象に関する報告書(記入済)
登録票(未入力のもの)
登録票(記入済のもの)
治験分担医師・協力者リスト(記入済のもの)
モニタリング手順書・計画書
各種治験の実施に関する手順書 等
模擬文書モニタリング用資材
初回申請時に必要な書式一式
治験に関する変更申請に必要な書式一式
重篤な有害事象等に関する報告書を提出する際に必要な書式一式
安全性情報等に関する書類を提出する際に必要な書式一式 等
| 研修資材のご利用について 氏名 ・所属 ・連絡先(メールアドレス)・利用目的(研修目的の場合は研修会名もしくは研修対象者) をメール本文に記入し、東北大学ネットワーク事務局(trnw-office(@)crieto.hosp.tohoku.ac.jp)までご連絡ください。 なお、利用目的等によっては、ご利用をお断りすることがあります。 また、ご利用いただく際は、後日、アンケート等をお願いする場合があります。 |
| 以下の資料は医療機関内の実際の運用に合うか確認してご利用ください。 手順書、計画書・報告書の雛形は適宜修正して使用してください。 また、手順書、計画書・報告書の作成にあたっては、「人を対象とする医学系研究に関する倫理指針(平成26年文部科学省・厚生労働省告示第3号)」並びに実施される臨床研究において適用される関連法規を遵守した内容になっているか必ずご確認ください。 なお、本資料は適宜改訂する予定ですので、ご了承ください。 本資料の利用によって発生したいかなる損害についても責任は負いません。 |
ポリシー
2015年12月作成。
アカデミアにおけるモニタリングの考え方、基本的概念を明示しました。
モニタリングの概念、アカデミアのあるべき研究実施体制の提言、品質管理に関する重要項目を掲載しています。
テンプレート
モニタリング手順書(倫理指針対応) 2015年12月作成
モニタリング手順書(臨床研究法対応) 2019年11月作成
モニタリング手順書(再生医療対応) 2019年11月作成
(参考資料:「再生医療等の安全性の確保等に関する法律」の報告の流れ 【出典:大阪大学認定再生医療等委員会事務局】)
本手順書テンプレートは、研究者が臨床研究を実施する際に、研究単位でのモニタリング実施手順を定める際に使用できます。本手順書の記載はあくまでも記載例であり、研究計画に応じて適宜修正を行ってください。
モニタリング計画書・報告書 2016年2月作成
本計画書はテンプレートです。ご使用の際は、研究計画及び手順書に基づき適宜修正を行ってください。
また、報告書の書式はあくまでも参考書式であり、書式の名称、レイアウト、記載内容等は、研究計画等に応じて適宜修正して使用してください。
パンフレット
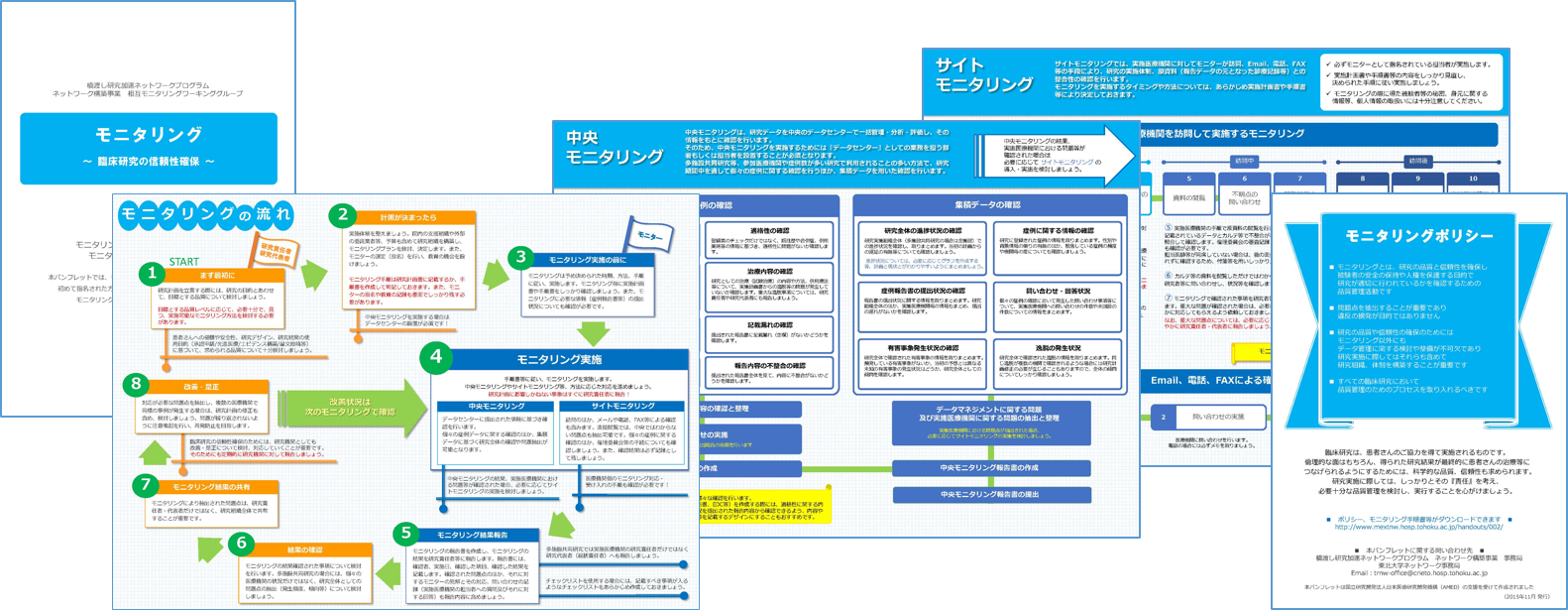
2015年11月発行。
モニタリングを実施する研究者、モニターとして初めて指名された方が主体的にモニタリングを実施できるよう、モニタリングの流れと基本事項を記載しています。
パンフレット第2弾。2018年2月発行。
モニタリングとその背景に関する基本的事項を整理・紹介しています。
モニタリングを実施する前の準備資料として、お役立てください。
なお、巻末に「参考」として臨床研究法に関する留意事項を記載しておりますが、「臨床研究法施行規則(案)(概要)2017年12月28日」をもとに作成していますので、今後発出される省令や通知等を必ずご確認ください。
これからモニタリングをするにあたって知っておきたい臨床研究法の基礎知識
パンフレット第3弾。2020年2月発行。 臨床研究法下で実施するモニタリングとその背景に関する基本的事項を、できるだけわかりやすく整理・紹介しています。
(第2版)